Какой объем можно выделить углекислого газа (CO2) при действии 200 грамм 10-процентного раствора азотной кислоты (HNO3) на 90 грамм мела, содержащего 8% нерастворимых в кислоте примесей?
Решение задачи
Напомню, что основу химического состава мела составляет карбонат кальция (CaCO3) с небольшим количеством примесей.
Запишем уравнение реакции выделить углекислый газ (CO2):
![]()
Вычислим, сколько азотной кислоты (HNO3) (в граммах) содержится в 200 грамм 10-процентного раствора азотной кислоты (HNO3) по формуле:
![]()
m (HNO3) = 200 г ⋅ 0,1 = 20 (г).
Если раствор 10-процентный, то массовая доля азотной кислоты (HNO3) в нем 0,1.
Учитывая, что мел содержит 8% примесей, следовательно, в состав мела входит 92% (0,92) карбоната кальция (CaCO3). Вычислим, сколько карбоната кальция (CaCO3) (в граммах) содержится в 90 грамм мела по формуле:
![]()
m (CaCO3) = 90 г ⋅ 0,92 = 82,8 (г).
Учитывая, что молярные массы азотной кислоты (HNO3) и карбоната кальция (CaCO3) соответственно равны 63 и 100 г/моль (смотри таблицу Менделеева), найдем химическое количество данных веществ по формуле:
![]()
Получаем:
n (HNO3) = 20 г / 63 г/моль = 0,32 (моль),
n (CaCO3) = 82,8 г / 100 г/моль = 0,83 (моль).
По уравнению реакции определим, какое вещество находится в избытке, а какое в недостатке. Напомню, расчет следует вести по недостатку.
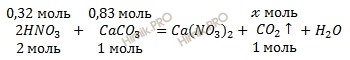
Из уравнения реакции следует, что на 1 моль карбоната кальция (CaCO3) требуется в 2 раза больше азотной кислоты (HNO3), то есть на 0,83 моль карбоната кальция (CaCO3) необходимо 1,66 азотной кислоты (HNO3), следовательно, 0,32 моль недостаточно для 0,83 карбоната кальция (CaCO3), который взят в избытке и прореагирует неполностью.
Так как карбонат кальция (CaCO3) взят в избытке, расчет следует вести по числу молей азотной кислоты (HNO3). Составим соотношение:
2 моль HNO3 надо, чтобы выделить углекислый газ 1 моль
0,32 моль HNO3 надо, чтобы выделить углекислый газ х моль
Откуда:
![]()
Вычислим объем углекислого газа (CO2), который выделяется в ходе реакции по формуле, устанавливающей связь между химическим количеством вещества и объемом:
![]()
V (CO2) = 0,16 моль ⋅ 22,4 л/моль = 3,58 (л).
Ответ:
выделить углекислый газ объемом 3,58 литра.

Всегда ли нужно вести расчет по недостатку?А если нам нужно было бы найти (в этой же задаче) нитрат кальция мы бы тоже рассчитывали по недостатку
Да, при решении задач такого типа расчет всегда ведем по веществу, данному в недостатке. Вещество, данное в недостатке в ходе химической реакции расходуется полностью. Для нахождения количества нитрата кальция (Ca(NO3)2) расчет так же ведем по недостатку (азотной кислоте (HNO3)).