В 200 граммах 5-процентного раствора хлорида бария (BaCl2) растворили 61 грамм дигидрат хлорида бария (BaCl2 ∙ 2H2O). Вычислите массовую долю хлорида бария (BaCl2) в растворе.
Решение задачи
I способ решения (II способ)
Вычислим, сколько хлорида бария (BaCl2) (в г) содержится в 200 г 5-процентного раствора. Составим соотношение:
в 100 г раствора содержится 5 г BaCl2
в 200 г раствора содержится ![]() г BaCl2
г BaCl2
Откуда:
![]()
Учитывая, что молярные массы дигидрат хлорида бария (BaCl2 ∙ 2H2O) и хлорида бария (BaCl2) соответственно равны 244 и 208 г/моль и что в 1 моль дигидрат хлорида бария (BaCl2 ∙ 2H2O) содержится 1 моль хлорида бария (BaCl2), найдем массы данных веществ по формуле, устанавливающей связь между массой и химическим количеством вещества:
![]()
Получаем:
m (BaCl2 ∙ 2H2O) = 1 моль ∙ 244 г/моль = 244 (г)
m (BaCl2) = 1 моль ∙ 208г/моль = 208 (г).
Найдем, сколько хлорида бария (BaCl2) (в г) содержится в 61 г кристаллогидрата (дигидрат хлорида бария (BaCl2 ∙ 2H2O)). Составим пропорцию:
в 244 г BaCl2 ∙ 2H2O содержится 208 г BaCl2
в 61 г BaCl2 ∙ 2H2O содержится ![]() г BaCl2
г BaCl2
Откуда:
![]()
Найдем массу конечного раствора по формуле:
m (конечного раствора) = m (исходного раствора) + m (кристаллогидрата)
Получаем:
m (конечного раствора) = 200 + 61 = 261 (г).
Найдем массу хлорида бария (BaCl2), которая содержится в 261 г раствора по формуле:
m (BaCl2 в конечном растворе) = m (BaCl2 в исходном растворе) + m (BaCl2 в кристаллогидрате)
m (BaCl2 в конечном растворе) = 10 + 52 = 62 (г).
Вычислим массовую долю хлорида бария (BaCl2) в конечном растворе по формуле:
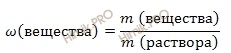
Массовая доля растворенного вещества в растворе – это отношение массы растворенного вещества к массе раствора. Выражается в долях единицы или в %. Следует отметить, что массовая доля растворенного вещества в растворе, выраженная в %, называется процентной концентрацией раствора.
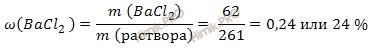
Ответ: массовая доля хлорида бария (BaCl2) в растворе равна 0,24.
