Для образования средней соли к 40 миллилитрам раствора серной кислоты (H2SO4) с плотностью 1,025 г/мл добавили 43,2 миллилитра 7,4-процентного раствора гидроксида калия (KOH) с плотностью 1,06г/мл. Рассчитайте массовую долю серной кислоты в растворе.
Решение задачи
Запишем уравнение реакции образования средней соли:
![]()
Рассчитаем массу раствора гидроксида калия (KOH) по формуле, устанавливающей связь между массой и объемом:
![]()
Получаем:
m (раствора KOH) = 43,2 ∙ 1,06 = 45,79 (г).
Массовая доля серной кислоты. Используя формулу нахождения массовой доли растворенного вещества:
![]()
выразим массу вещества:
![]()
Получаем:
m (вещества KOH) = 45,79 ∙ 0,074 = 3,39 (г).
Если раствор 7,4-процентный, то массовая доля гидроксида калия (KOH) в нем 0,074.
Массовая доля серной кислоты. Учитывая, что молярные массы гидроксида калия (KOH) и серной кислоты (H2SO4) соответственно равны 56 г/моль и 98 г/моль (смотри таблицу Менделеева), по уравнению реакции образования средней соли рассчитаем, сколько грамм серной кислоты (H2SO4) нужно для нейтрализации 3,39 г гидроксида калия (KOH):
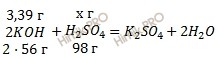
на реакцию нейтрализации 112 г KOH нужно 98 г H2SO4
на реакцию нейтрализации 3,39 г KOH нужно х г H2SO4
Откуда:
![]()
Рассчитаем массу раствора серной кислоты (H2SO4) по формуле, устанавливающей связь между массой и объемом:
![]()
Получаем:
m (раствора H2SO4) = 40 ∙ 1,025 = 41 (г).
Массовая доля растворенного вещества в растворе – это отношение массы растворенного вещества к массе раствора. Выражается в долях единицы или в %.
Рассчитаем массовую долю серной кислоты в растворе:
![]()
Получаем, массовая доля серной кислоты равна:
w (H2SO4) = 2,97 / 41 = 0,072 или 7,2%
Ответ:
массовая доля серной кислоты равна 7,2 %.
