Рассчитать массу и объем газа, образовавшегося при горении пропана (C3H8) массой 8,8 грамм.
Решение задачи
Запишем реакцию горения пропана (C3H8):
![]()
Учитывая, что молярные массы пропана (C3H8) и углекислого газа (CO2) соответственно равны 44 г/моль и 44 г/моль, по уравнению реакции, найдем массу углекислого газа (CO2), который образуется при полном горении пропана (C3H8):
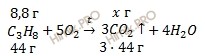
при горении пропана (C3H8) 8,8 г образуется x г CO2
при горении пропана (C3H8) образуется 1 г CO2
Откуда:
![]()
Учитывая, что пропан (C3H8) – газ, вычислим объем углекислого газа (CO2), который образуется при полном горении пропана (C3H8), по формуле перерасчета, устанавливающей связь между массой и объемом газа:
![]()
Получаем:
V (C3H8) = 26,4 ∙ 22,4 / 44 = 13,44 (л).
Ответ:
масса углекислого газа равна 26,4 грамма,
объем углекислого газа равен 13,44 литра.
