В результате полного окисления глюкозы (C6H12O6) выделилось 44,8 литра углекислого газа (CO2) (нормальные условия). Определить массу полного окисления глюкозы.
Решение задачи
Запишем уравнение реакции полного окисления глюкозы (C6H12O6):
![]()
Учитывая, что углекислый газ (CO2) – бесцветный газ, вычислим массу углекислого газа (CO2), по формуле перерасчета, устанавливающей связь между объемом газа и массой:
![]()
Рассчитаем молярную массу углекислого газа (CO2), используя данные таблицы Менделеева:
M (CO2) = 12 + 2 ⋅ 16 = 44 (г/моль).
Известные данные подставим в формулу, получаем:
m (CO2) = 44 ∙ 44,8 / 22,4 = 88 (г).
Рассчитаем молярную массу глюкозы (C6H12O6), используя данные таблицы Менделеева:
M (C6H12O6) = 6 ⋅ 12 + 1 ⋅ 12 + 6 ⋅ 16 = 180 (г/моль).
Из уравнения реакции полного окисления глюкозы (C6H12O6) найдем массу глюкозы:
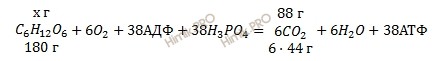
при полном окислении глюкозы х г образуется 88 г CO2
при полном окислении глюкозы 180 г образуется 264 г CO2
Откуда:
![]()
Ответ:
масса полного окисления глюкозы равна 60 грамм.
