Если выход бензола (C6H6) 75 %, то из 67,2 литров ацетилена (C2H2) при тримеризации получение бензола (C6H6) массой?
Решение задачи
Запишем уравнение получения бензола путем тримеризации ацетилена (C2H2) – реакция Зелинского:
![]()
Напомню, что под выходом продукта реакции понимают отношение массы (объема, числа молей) практически полученного вещества к массе (объему, числу молей), теоретически рассчитанной по уравнению реакции.
Найдем химическое количество ацетилена (C2H2) нужное для получения бензола по формуле, устанавливающей связь между химическим количеством вещества и объемом:
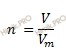
Получаем:
n (C2H2) = 67,2 / 22,4 = 3 (моль).
По уравнению реакции найдем химическое количество бензола (C6H6) (теоретическое), который образуется при тримеризации ацетилена (C2H2):
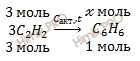
из 3 моль C2H2 образуется 1 моль бензола (C6H6)
из 3 моль C2H2 образуется х моль бензола (C6H6)
Откуда:
![]()
Учитывая, что молярная масса бензола (C6H6) равна 78 г/моль (смотри таблицу Менделеева), по формуле, устанавливающей связь между химическим количеством вещества и массой, рассчитаем теоретическую массу бензола (C6H6), который образуется в ходе реакции получения бензола:
![]()
Получаем:
mтеор.(C6H6) = 1 ∙ 78 = 78 (г).
Рассчитаем практическую массу получения бензола (C6H6) по формуле:
![]()
mпракт.(C6H6) = 75 ⋅ 78 / 100 = 58,5 (г).
Ответ:
образуется бензол массой 58,5 грамм.
