Хлорид металла содержит 69% хлора (Cl), атомная масса металла равна 47,90. Вычислите эквивалентную массу металла и его валентность.
Решение задачи
Зная, что атомная масса металла равна 47,90, воспользовавшись периодической системой химических элементов Д.И. Менделеева, находим, что искомый металл – титан (Ti).
Приняв массу хлорида за 100%, найдем массовую долю титана (Ti) в хлориде.
Получаем:
w (Ti) = 100 – 69 =31 (%).
Таким образом, на 69 частей массы хлора (Cl) приходится 31 часть массы титана (Ti) или на 69 г хлора (Cl) приходится 31 г титана (Ti).
Учитывая, что эквивалентная масса хлора (Cl) равна 35,5 г/моль, определим эквивалентную массу металла (титана (Ti)) в хлориде по закону эквивалентов:
![]()
Откуда выразим эквивалентную массу металла (титана (Ti)) в хлориде:
![]()
Получаем:
M экв (Ti) = 31 ∙ 35,5/69 = 16 (г/моль).
Валентность титана (Ti) находим из соотношения:
![]()
Отсюда:
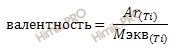
Получаем:
валентность = 47,9/16 = 3
Следовательно, металл – трехвалентный титан.
Ответ:
эквивалентная масса металла равна 16 г/моль;
валентность равна 3.
