К 400 грамм 10-процентного раствора нитрата кальция (Ca(NO3)2) добавили 100 грамм воды. Вычислите массовую долю вещества в растворе нитрата кальция (Ca(NO3)2).
Решение задачи
I способ решения (II способ)
Найдем, какая масса нитрата кальция (Ca(NO3)2) (в граммах) содержится в 400 г 10-процентного раствора. Составим пропорцию:
в 100 г раствора содержится 10 г (Ca(NO3)2)
в 400 г раствора содержится х г (Ca(NO3)2)
Откуда:
![]()
Масса полученного раствора равна:
400 + 100 = 500 (г).
Учитывая, что после добавления воды 40 г нитрата кальция (Ca(NO3)2) содержится в 500 г полученного раствора, найдем массовую долю вещества в растворе нитрата кальция (Ca(NO3)2):
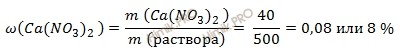
Ответ:
массовая доля вещества в растворе нитрата кальция (Ca(NO3)2) 0,08.
