Чему равен титр THCl/CaO, если на титрование 0,1144 грамм карбоната кальция (CaCО3) затрачено 27,65 миллилитра раствора соляной кислоты (HCl).
Решение задачи
По условию задачи нужно определить титр по оксиду кальция (СаО), а не по карбонату кальция (СаСО3), следовательно, вычислим скольким г оксида кальция (СаО), соответствует 0,1144 г карбоната кальция (СаСО3).
Учитывая, что молярные массы оксида кальция (СаО) и карбоната кальция (СаСО3) соответственно равны 56 г/моль и 100 г/моль (смотри таблицу Менделеева), составим пропорцию:
М (СаО) — М (СаСОз)
х — 0,1144
Получаем:
m (СаО) = 56 ⋅ 0,1144 /100 = 0,0641 (г).
Титр можно вычислить по определяемому веществу. Эту величину еще называют условным титром:
Где:
m (b) – масса вещества b (в граммах), которое взаимодействует с данным раствором;
V (a) – объем раствора вещества a (в миллилитрах).
Так как на титрование 0,0641 г оксида кальция (СаО) идет 27,65 мл соляной кислоты (HCl), то титр равен THCl/CaO:
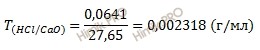
Ответ:
титр равен 0,002318 г/мл.
