Сплав алюминия и магния массой 3,00 грамма смешивают с избытком оксида хрома (III) (Cr2O3) и поджигают. В результате образуется хром (Cr) массой 5,55 грамм. Определите состав сплава алюминия и магния (ω, %).
Решение задачи
Запишем уравнения реакций получения хрома (Cr) металлотермией при смешении сплава алюминия и магния:
![]()
![]()
Металлотермия – когда более активные металлы вытесняют (восстанавливают) менее активные из их оксидов.
Учитывая, что молярные массы алюминия (Al), магния (Mg) и хрома (Cr) соответственно равны 27 г/моль, 24 г/моль и 52 г/моль (смотри таблицу Менделеева), обозначим содержание магния (Mg) в сплаве алюминия и магния через х грамм. Тогда содержание алюминия (Al) в сплаве алюминия и магния составит (3 — х) грамм.
Обозначим массу хрома (Cr), образующегося в уравнении (1) a грамм, в уравнении (2) b грамм:
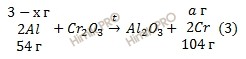
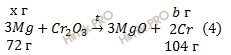
Из уравнений (3,4) следует, что масса образующегося хрома (Cr) «а» составит:
а = 104 ⋅ (3 – х) / 54 (г),
масса хрома (Cr) «b» составит:
b = 104 ⋅ х / 72 (г).
По условию задачи масса хрома (Cr) 5,55 г, то есть:
а + b = 5,55 г.
Отсюда:
104 ⋅ (3 — х) / 54 + 104 ⋅ х / 72 = 5,55
5,78 – 1,93 х + 1,44 х = 5,55
0,49 х = 0,23
х = 0,47 (г).
Следовательно, масса магния (Mg) 0,47 грамма.
Найдем массу алюминия (Al):
m (Al) = 3 – 0,47 = 2,53 (г).
Используя формулу нахождения массовой доли вещества:
![]()
Рассчитаем массовую долю магния (Mg):
w (Mg) = 0,47 ⋅ 100% / 3 = 15,67 (%).
Тогда массовая доля алюминия (Al) равна:
100% — 15,67% = 84,33 (%).
Ответ:
состав сплава алюминия и магния – магний 15,67%, алюминий 84,33%.

Огромнейшее Вам спасибо!!!!
Рада помочь!