Вычислить рН раствора, содержащего 0,001 М НСl.
Решение задачи
Запишем уравнение диссоциации соляной кислоты (HCl):
![]()
Вычислить рН раствора
Учитывая, что раствор соляной кислоты 0,001 M по уравнению диссоциации вычислим, сколько моль ионов водорода H+ образуется при полной диссоциации 0,001 моль соляной кислоты (HCl):
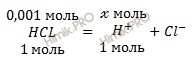
при диссоциации 1 моль HCl образуется ионов H+
при диссоциации 0,01 моль HCl образуется х моль ионов H+
Откуда:
![]()
Напомню, молярная концентрация – число молей вещества содержащегося в единице объема раствора.
Следовательно, концентрация ионов водорода равна:
![]()
Вычислить pH раствора по формуле:
![]()
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
Получаем вычислить рН раствора:
![]()
Ответ:
рН раствора соляной кислоты 3.

good job
Thanks!