К 400 миллилитрам 28-процентного раствора серной кислоты (H2SO4) (плотность раствора равна 1,2 г/см3) добавили 200 миллилитров 10-процентного раствора (плотность раствора равна 1,07 г/см3) этого же вещества. Какова массовая доля серной кислоты (H2SO4) в растворе?
Решение задачи
III способ решения (I способ, II способ)
При решении данной задачи можно применить правило креста.
Правило креста (диагональная модель «конверта Пирсона») – диагональная схема правила смешения:

При расчетах слева на концах отрезков записывают массовые доли растворенного вещества в исходных растворах (ω1, ω2), на пересечении отрезков – массовую долю растворенного вещества в растворе, который нужно приготовить, справа (на концах отрезков) – разность: вычитают по диагонали из большего меньшее значение. Получаемые значения (массовые части) показывают, в каком соотношении надо слить исходные растворы.
Перед тем как составить диагональную схему необходимо найти массу 1 и 2 растворов.
Найдем массу 1 раствора серной кислоты (H2SO4) по формуле:
![]()
Получаем:
m1 (раствора) = 1,2 г/см3 ∙ 400 см3 =480 (г).
Найдем массу 2 раствора серной кислоты (H2SO4) по формуле:
![]()
Получаем:
m2 (раствора) = 1,07 2 г/см3 ∙ 200 см3 = 214 (г).
Составим диагональную схему и найдем массовую долю серной кислоты в конечном растворе:
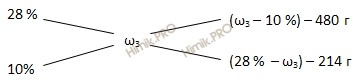
Получаем пропорцию:
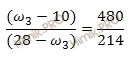 Решаем:
Решаем:
214 ∙ (ω3 – 10) = 480 ∙ (28 – ω3)
214 ω3 – 2140 = 13440 – 480 ω3
694 ω3 = 15580
ω3 = 22 % или 0,22.
Ответ: массовая доля серной кислоты в растворе = 0,22.
