При термическом разложении метана (CH4) количеством вещества 14 моль получен ацетилен (C2H2), объем которого при нормальных условиях составил 120,96 литра. Вычислите объемную долю (%) выхода ацетилена (C2H2).
Решение задачи
Запишем уравнение реакции разложения метана (CH4):
![]()
По уравнению реакции разложения метана найдем химическое количество ацетилена (C2H2) (теоретический выход), который выделяется в ходе реакции разложения метана:
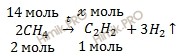
из 14 моль разложения метана (CH4) образуется х моль C2H2
из 2 моль разложения метана (CH4) образуется 1 моль C2H2
Откуда:
![]()
По формуле, устанавливающей связь между химическим количеством вещества и объемом, вычислим объем ацетилена (C2H2), который образуется в ходе реакции разложения метана (CH4):
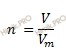
Получаем:
V теор.( C2H2) = 7 моль ∙ 22,4 л/моль = 156,8 (л).
Напомню, что под выходом продукта реакции понимают отношение массы (объема, числа молей) практически полученного вещества к массе (объему, числу молей), теоретически рассчитанной по уравнению реакции.
Находим объемную долю выхода ацетилена (C2H2), который образуется в результате разложения метана (CH4), по формуле:
![]()
Получаем:
![]()
Ответ:
объемная доля выхода ацетилена 77,14%.
