Рассчитайте массу воды (H2O), образующейся при взрыве смеси водорода (H2) массой 2 грамма и кислорода (O2) массой 12 грамм.
Решение задачи
Перед решением задачи, напомню, что вещества вступают в реакцию в определенных стехиометрических отношениях. Если для реакции взяты вещества в отношениях, не соответствующих стехиометрическим, то одно из них окажется в избытке. Масса образовавшегося продукта определяется по массе исходного вещества, прореагировавшего полностью. Такие задачи относят к задачам на избыток-недостаток.
Cоставим уравнение реакции образования воды:
![]()
Из уравнения реакции следует, что водород (H2) и кислород (O2) взаимодействуют в молярном отношении 2 : 1.
Найдем, какое из веществ, вступивших в реакцию, дано в избытке, а какое – в недостатке. Для этого найдем химическое количество веществ и сопоставим их с соотношением количеств этих веществ в уравнении реакции. Воспользуемся формулой, устанавливающей связь между химическим количеством вещества и массой:
![]()
Получаем:
![]()
![]()
Следовательно, водород взят в избытке (1 : 0,375 = 2,667 : 1).
Далее расчет проводим по кислороду (O2) – веществу, взятому в недостатке.
Рассчитаем молярные массы веществ, вступивших в реакцию:
M (H2O) = 2 + 16 = 18 (г/моль)
M (O2) = 2 ∙ 16 = 32 (г/моль)
Согласно уравнению реакции найдем, какая масса воды образуется при участии 12 грамм кислорода (O2):
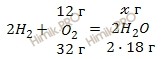
при взаимодействии 12 г O2 с H2 образуется ![]() г H2O
г H2O
при взаимодействии 32 г O2 с H2 образуется 36 г H2O
Откуда:
![]()
Следовательно, масса воды (H2O), образующейся при взрыве смеси водорода (H2) и кислорода (O2) равна 13,5 грамм.
Ответ:
масса воды равна 13,5 грамм.
