Какой объём водорода выделился при взаимдействии 10,58 мл 16% раствора соляной кислоты (ρ = 1,078 г/мл) с 1,12 г железа? Хватит ли такого количества соляной кислоты для полного растворения железа?
Решение задачи
Запишем уравнение реакции взаимодействия железа (Fe) с соляной кислотой (HCl):
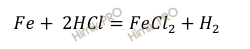
Вычислим массу 10,58 мл 16-процентного раствора соляной кислоты (HCl).
Найдем, массу раствора соляной кислоты (HCl) по формуле, устанавливающей связь между массой и объемом раствора:
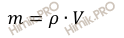
mр-ра (HCl) = 1,078 г/мл ∙ 10,58 мл = 11,405 (г).
Найдем, сколько в растворе содержится соляной кислоты (HCl) (в г). Для расчета будем использовать формулу нахождения массовой доли растворенного вещества в растворе:
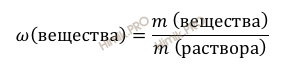
Массовая доля растворенного вещества в растворе – это отношение массы растворенного вещества к массе раствора. Выражается в долях единицы или в %. Следует отметить, что массовая доля растворенного вещества в растворе, выраженная в %, называется процентной концентрацией раствора.
Откуда выразим m (вещества):

Получаем:
m (HCl) = 11,405 ∙ 0,16 = 1,825 (г).
Если раствор 16-процентный, то массовая доля соляной кислоты (HCl) в нем 0,16.
Учитывая, что молярная масса соляной кислоты (HCl) и железа (Fe) соответственно равны 36,5 г/моль и 56 г/моль (смотри таблицу Д.И. Менделеева), рассчитаем химическое количество железа (Fe) и соляной кислоты (HCl) в растворе, используя формулу, которая устанавливает связь между химическим количеством вещества и массой:
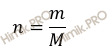
Получаем:
n (HCl) = 1,825/36,5 = 0,05 (моль).
n (Fe) = 1,12/56 = 0,02 (моль).
По уравнению реакции найдем, сколько соляной кислоты (HCl) (в молях) нужно для полного растворения 1,12 г железа (Fe):
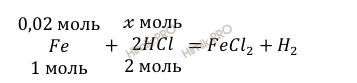
х моль HCl растворяет 0,02 моль Fe
2 моль HCl растворяет 1 моль Fe
Откуда:
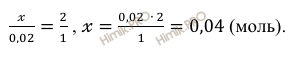
Это означает, что соляная кислота (HCl) находится в избытке и дальнейшие расчеты производим по железу.
Согласно уравнению реакции растворения железа химическое количество водорода (H2), который выделился железа (Fe) равно химическому количеству железа (Fe):
n (H2) = n (Fe) = 0,02 (моль).
По формуле, устанавливающей связь между химическим количеством вещества и объемом, найдем объем водорода (H2), который выделился в ходе реакции растворения железа:
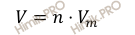
Получаем:
V (H2) = 0,02 ∙ 22,4 = 0,448 (л).
Ответ:
раствора соляной кислоты хватит;
объем водорода 0,448 литра.
