Константа кристаллической решетки хлорида калия (KCl) равна 3,16 ⋅ 10-10 м. Рассчитайте эффективный радиус иона калия (K+), если радиус иона хлора (Cl—) равен 1,811 ⋅ 10-10 м.
Решение задачи
Вспомним, что расстояние между центрами двух соседних структурных частиц в кристаллической решетке называют константой решетки.
Если исходить из предположения, что структурные частицы кристалла – касающиеся друг друга шары, то константа решетки равна сумме радиусов этих частиц.
Радиусы ионов (или атомов), определяемые при таком допущении, называют эффективными радиусами, так как они являются радиусами сфер действия ионов (или атомов):
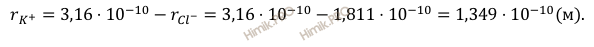
Ответ:
эффективный радиус иона калия равен 1,349 ⋅ 10-10 м.
