Раствор соляной кислоты (HCl) объемом 1,8 мл (плотность 1,18 г/мл) с массовой долей вещества 36 процентов, разбавили водой до 1 литра. Найти pH раствора полученного?
Решение задачи
Запишем уравнение диссоциации соляной кислоты:
![]()
Вычислим массу 1,8 мл 36-процентного раствора соляной кислоты (HCl).
Найдем, массу раствора соляной кислоты (HCl) по формуле, устанавливающей связь между массой и объемом раствора:
![]()
m = 1,18 г/мл ∙ 1,8 мл = 2,124 (г).
Найдем, сколько в растворе содержится соляной кислоты (HCl) (в г). Для расчета будем использовать формулу нахождения массовой доли растворенного вещества в растворе:
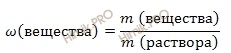
Массовая доля растворенного вещества в растворе – это отношение массы растворенного вещества к массе раствора. Выражается в долях единицы или в %. Следует отметить, что массовая доля растворенного вещества в растворе, выраженная в %, называется процентной концентрацией раствора.
Откуда выразим m (вещества):
![]()
Получаем:
m (HCl) = 2,124 ∙ 0,36 = 0,765 (г).
Если раствор соляной кислоты (HCl) 36-процентный, то массовая доля соляной кислоты (HCl) в нем 0,36.
Учитывая, что молярная масса соляной кислоты (HCl) равна 36,5 г/моль, рассчитаем химическое количество соляной кислоты (HCl) в растворе, используя формулу, которая устанавливает связь между химическим количеством вещества и массой:
![]()
Получаем:
n (HCl) = 0,765/36,5 = 0,021 (моль).
Учитывая, что объем раствора разбавили водой (H2O) до 1 л, найдем молярную концентрацию раствора соляной кислоты (HCl) по формуле:
![]()
Молярная концентрация показывает количество растворенного вещества (моль), содержащегося в 1 л раствора.
Получаем:
![]()
По уравнению диссоциации вычислим, сколько моль ионов водорода (H+)образуется при полной диссоциации 0,021 моль раствора соляной кислоты (HCl):
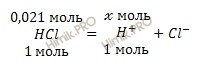 при диссоциации 1 моль HCl образуется 1 моль ионов H+
при диссоциации 1 моль HCl образуется 1 моль ионов H+
при диссоциации 0,021 моль HCl образуется ![]() моль ионов H+
моль ионов H+
Откуда:
![]()
Следовательно, концентрация ионов водорода ([H+]) равна 0,021 моль.
Вычислим pH раствора соляной кислоты (HCl) по формуле:
![]()
Водородный показатель (pH) раствора численно равен отрицательному десятичному логарифму концентрации ионов водорода в этом растворе.
Получаем:
![]()
![]()
Ответ:
pH раствора 1,678.
