В каком направлении сместится химическое равновесие, если концентрацию всех реагирующих веществ увеличить в 2 раза? Реакция протекает по уравнению: 4HCl + O2 = 2H2O +2Cl2.
Решение задачи
Уравнение реакции имеет вид:
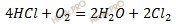
Первоначальные скорости прямой и обратной реакций были следующие:
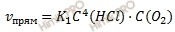
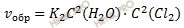
После увеличения концентраций скорость прямой реакции была:
𝑣прям = K1 ⋅ (2C (HCl))4 ⋅ 2C(O2) = 25 ⋅ K1 ⋅ C4 (HCl) ⋅ C(O2) = 32 ⋅ K1 ⋅ C4 (HCl) ⋅ C(O2)
То есть скорость прямой реакции выросла в 32 раза.
После увеличения концентраций скорость обратной реакции была:
𝑣обр = K2 ⋅ (2C (H2O))2 ⋅ (2C(Cl2))2 = 24 ⋅ K2 ⋅ C2 (H2O) ⋅ C(Cl2) = 16 ⋅ K2 ⋅ C2 (H2O) ⋅ C(Cl2)
То есть скорость обратной реакции выросла в 16 раз.
В каком направлении сместится химическое равновесие.
Следовательно, равновесие сместится в сторону прямой реакции.
Ответ:
химическое равновесие сместится в сторону прямой реакции.
