Какое количество хлорида кальция (CaCl2) образуется в результате взаимодействия оксида кальция (CaO) с соляной кислотой (HCl) массой 146 грамм.
Решение задачи
Запишем уравнение реакции взаимодействия оксида кальция (CaO) с соляной кислотой (HCl):
![]()
Учитывая, что молярная масса соляной кислоты (HCl) равна 36,5 г/моль (смотри таблицу Менделеева), найдем химическое количество соляной кислоты (HCl) по формуле, устанавливающей связь между химическим количеством вещества и массой:
![]()
Получаем:
n (HCl) = 146 /36,5 = 4 (моль).
По уравнению реакции найдем химическое количество хлорида кальция (CaCl2), который образуется в ходе реакции:
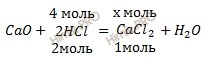
при действии 4 моль HCl образуется х моль CaCl2
при действии 2 моль HNO3 образуется 1 моль CO2
Откуда:
![]()
Следовательно, в ходе реакции образовалось количество хлорида кальция (CaCl2) 2 моль.
Ответ:
количество хлорида кальция 2 моль.
