В 1 литре раствора содержится 0,1 моль хлорида калия (KCl) и 0,05 моль карбоната натрия (Na2CO3). Сколько хлорида натрия (NaCl) и карбоната калия (K2CO3) (в моль) нужно взять, чтобы приготовить 1 литр раствора такого же состава? Запишите уравнение диссоциации соли.
Решение задачи
Запишем уравнение диссоциации соли хлорида калия (KCl):
![]()
По диссоциации соли уравнению вычислим, сколько моль ионов калия (K+) и хлора (Cl—) образуется при полной диссоциации 0,1 моль хлорида калия (KCl):

при диссоциации соли 1 моль хлорида калия (KCl) образуется ионов K+
при диссоциации соли 0,1 моль хлорида калия (KCl) образуется х моль ионов K+
Откуда:
![]()
при диссоциации соли 1 моль хлорида калия (KCl) образуется ионов Cl—
при диссоциации соли 0,1 моль хлорида калия (KCl) образуется y моль ионов Cl—
Откуда:
![]()
Запишем уравнения диссоциации соли карбоната натрия (Na2CO3):
![]()
По уравнению диссоциации вычислим, сколько моль ионов натрия (Na+)и карбонат-ионов (CO32-) образуется при полной диссоциации 0,05 моль карбоната натрия (Na2CO3):
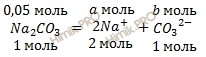
при диссоциации соли 1 моль карбоната натрия (Na2CO3) образуется 2 моль ионов Na+
при диссоциации соли 0,05 моль карбоната натрия (Na2CO3) образуется a моль ионов Na+
Откуда:
![]()
при диссоциации соли 1 моль карбоната натрия (Na2CO3) образуется 1 моль ионов CO32-
при диссоциации соли 0,05 моль карбоната натрия (Na2CO3) образуется b мольионов CO32-
Откуда:
![]()
Запишем уравнения диссоциации солей хлорида натрия и карбоната калия:
![]()
![]() Чтобы при замене солей число ионов не изменилось, в растворе должно содержаться, как следует из уравнения диссоциации соли:
Чтобы при замене солей число ионов не изменилось, в растворе должно содержаться, как следует из уравнения диссоциации соли:

0,1 моль хлорида натрия (NaCl),

и 0,05 моль карбоната калия (K2CO3).
Ответ:
0,1 моль хлорида натрия;
0,05 моль карбоната калия.
