Какой объем 5-процентного раствора серной кислоты (H2SO4) (ρ = 1,07 г/мл) потребуется для полного растворения 2,7 грамм алюминия (Al)?
Решение задачи
Запишем уравнение реакции действия серной кислоты (H2SO4) на алюминий (Al):
![]() Учитывая, что молярные массы серной кислоты (H2SO4) и алюминия (Al) соответственно равны 98 г/моль и 27 г/моль, по уравнению реакции рассчитаем, сколько грамм серной кислоты (H2SO4) необходимо для растворения 2,7 грамм алюминия (Al):
Учитывая, что молярные массы серной кислоты (H2SO4) и алюминия (Al) соответственно равны 98 г/моль и 27 г/моль, по уравнению реакции рассчитаем, сколько грамм серной кислоты (H2SO4) необходимо для растворения 2,7 грамм алюминия (Al):
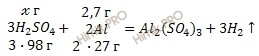
в 294 г H2SO4 можно растворить 54 г Al
в ![]() г H2SO4 можно растворить 2,7 г Al
г H2SO4 можно растворить 2,7 г Al
Откуда:
![]()
Используя формулу нахождения массовой доли растворенного вещества:
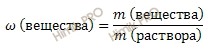 выразим массу раствора серной кислоты (H2SO4):
выразим массу раствора серной кислоты (H2SO4):
![]()
Получаем:
m (раствора H2SO4) = 14,7/ 0,05 = 294 (г).
Если раствор 5-процентный, то массовая доля серной кислоты (H2SO4) в нем 0,05.
Далее, по формуле, устанавливающей связь между массой раствора и объемом раствора, найдем объем раствора серной кислоты (H2SO4):
![]()
Получаем:
V (раствора H2SO4) = 294/1,07 = 274,77 (мл).
Ответ:
объем раствора серной кислоты (H2SO4) равен 274,77 миллилитра.
