Рассчитайте объем оксида серы (IV) (SO2) (нормальные условия), который можно получить при действии 0,05 литра 0,85 нормального раствора серной кислоты (H2SO4) на раствор сульфита калия (K2SO3).
Решение задачи
Запишем уравнение реакции действия раствора серной кислоты (H2SO4) на раствор сульфита калия (K2SO3):
![]()
Напомню, что под нормальной концентрацией понимают количество грамм-эквивалентов данного вещества, содержащегося в 1 л раствора. Нормальную концентрацию выражают в моль-экв/л или используют сокращение «н», «N»
![]() Рассчитаем молярную массу эквивалента серной кислоты (H2SO4) по формуле:
Рассчитаем молярную массу эквивалента серной кислоты (H2SO4) по формуле:
![]()
Напомню то, что молярная масса эквивалента – это масса одного моль эквивалента вещества, равная произведению фактора эквивалентности на молярную массу вещества.
![]()
Фактор эквивалентности (fэкв) – число, показывающее какая доля частицы (атома, молекулы) этого вещества равноценна одному иону водорода (H+) в реакциях обмена или одному электрону в окислительно-восстановительных реакциях.
Учитывая, что молярная масса серной кислоты (H2SO4) равна 98 г/моль, получаем:
![]()
Определим массу серной кислоты (H2SO4) в заданном объеме по формуле:
![]() Получаем:
Получаем:
m (H2SO4) = 0,05 ∙ 49 ∙ 0,85 =2,0825 (г).
По формуле, устанавливающей связь между химическим количеством вещества и массой, найдем химическое количество серной кислоты:
![]()
Получаем:
n (H2SO4) = 2,0825 /98 = 0,02125 (моль).
По уравнению реакции найдем химическое количество оксида серы (IV) (SO2), который выделяется в ходе реакции:
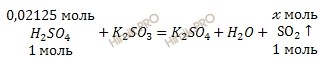
1 моль H2SO4 участвует в образовании 1 моль SO2
0,02125 моль H2SO4 участвует в образовании ![]() моль SO2
моль SO2
Откуда:
![]()
По формуле, устанавливающей связь между химическим количеством вещества и объемом, рассчитаем объем оксида серы (IV) (SO2), который образуется в ходе реакции:
![]() Получаем:
Получаем:
V (SO2) = 0,02125 ∙ 22,4 = 0,476 (л).
Ответ:
объем оксида серы (IV) (SO2) равен 0,476 литра.
