Чему равна нормальность 10-процентного (по массе) раствора йодата калия (KIO3), плотность которого равна 1,052 г/мл, если он восстанавливается до свободного йода?
Решение задачи
I способ решения (II способ)
Напомню, что под нормальной концентрацией понимают количество грамм-эквивалентов данного вещества, содержащегося в 1 л раствора. Нормальную концентрацию выражают в моль-экв/л или используют сокращение «н», «N».
Таким образом, для вычисления нормальности раствора йодата калия (KIO3) необходимо знать, сколько граммов йодата калия (KIO3) содержится в 1 л раствора.
Учитывая, что раствор йодата калия (KIO3) 10-процентный, следовательно, в 100 г раствора содержится 10 г вещества йодата калия (KIO3). Рассчитаем объем, который занимает данное весовое количество раствора йодата калия (KIO3), используя формулу:
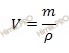
Получаем:
![]()
Вычислим, сколько грамм йодата калия (KIO3) содержится в 1 литре (1 л = 1000 мл) раствора. Составим соотношение:
в 95,057 мл раствора содержится 10 г KIO3
в 1000 мл раствора содержится ![]() г KIO3
г KIO3
Откуда:
![]()
Вычислим нормальность 10-процентного раствора йодата калия (KIO3), по формуле:
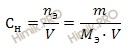
Рассчитаем молярную массу йодата калия (KIO3):
M (KIO3) = 39 + 127 + 3 ∙ 16 = 214 (г/моль).
Рассчитаем молярную массу эквивалента йодата калия (KIO3) по формуле:
![]()
Фактор эквивалентности (fэкв) – число, показывающее какая доля частицы (атома, молекулы) этого вещества равноценна одному иону водорода (H+) в реакциях обмена или одному электрону в окислительно-восстановительных реакциях.
Учитывая, что по условию задачи йодат калия (KIO3) восстанавливается до свободного йода:
![]()
следовательно, fэкв = 1/5, рассчитаем молярную массу эквивалента йодата калия (KIO3):
MЭ (KIO3) = 214 ∙ 1/5 = 42,8 (г/моль).
Вычислим нормальность 10-процентного раствора йодата калия (KIO3):
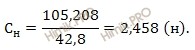
Ответ: нормальность йодата калия = 2,458 моль-экв/л.
