Смешали оксид кальция (CaO) массой 150 грамм с оксидом серы (VI) (SO3). Какая соль получится? Найти массу полученной соли, если оксид серы (VI) (SO3) взяли в избытке.
Решение задачи
Учитывая, что оксид кальция (CaO) относится к основным оксидам, он реагирует с кислотными оксидами (например, с оксидом серы (VI) (SO3)), образуя соли. Cоставим уравнение реакции оксида кальция (CaO) с оксидом серы (VI) (SO3):
![]()
Из уравнения реакции следует, что оксид кальция (CaO) и оксид серы (VI) (SO3) взаимодействуют в молярном отношении 1 : 1. В ходе реакции образуется соль – сульфат кальция.
Учитывая, что по условию задачи оксид серы (VI) (SO3) взяли в избытке, дальнейший расчет будем вести по веществу, взятому в недостатке – оксиду кальция (CaO).
Рассчитаем молярные массы оксида кальция (CaO) и сульфата кальция (CaSO4):
M (CaO) = 40 + 16 = 56 (г/моль),
M (CaSO4) = 40 + 32 + 4 ∙ 16 = 136 (г/моль).
Учитывая, что молярные массы оксида кальция (CaO) и сульфата кальция (CaSO4) соответственно равны 56 и 136 г/моль, вычислим массы данных веществ по формуле, устанавливающей связь между массой и химическим количеством вещества:
![]()
Учитывая количество моль из уравнения реакции получаем:
m (CaO) = 1 моль ∙ 56 г/моль = 56 (г)
m (CaSO4) = 1 моль ∙ 136 г/моль = 136 (г).
По уравнению реакции рассчитаем, какая масса соли образуется при участии 150 г оксида кальция (CaO):
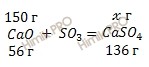
при участии 150 г CaO образуется ![]() г CaSO4
г CaSO4
при участии 56 г CaO образуется 136 г CaSO4
Откуда:
![]()
Следовательно, масса полученной соли сульфата кальция (CaSO4) равна 364,3 грамма.
Ответ:
масса сульфата кальция равна 364,3 грамма.
